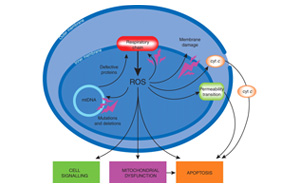
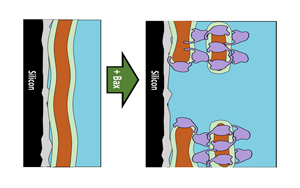
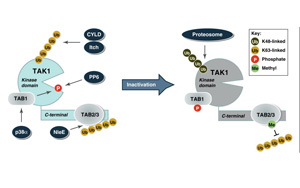
長期以來,研究人員一直認為,一旦細胞開始分化,長成皮膚細胞、肝細胞或神經元,這條道路就無法改變。但在過去的二十年里,科學家們意識到這條途徑要復雜得多。現在,密歇根大學(University of Michigan)的一個研究小組以斑馬魚為模型,發現人體線粒體(細胞內為身體產生能量的細胞器)中的一個環可能允許細胞在分化的道路上后退。他們的研究結果發表在《美國國家科學院院刊》上。
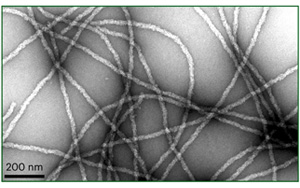
一個高度不穩定的蛋白質導致神經退化
EPFL的科學家們重現了在患有盧伽雷氏病和其他神經系統疾病的患者大腦中發現的病理蛋白聚集體的關鍵特征,為潛在的機制提供了見解,并為新療法提供了有希望的途徑。研究結果發表在《Nature Neuroscience》雜志上。
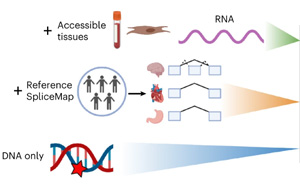
Nature Genetics:人類組織的異常剪接預測
到目前為止,還無法解釋大約一半罕見遺傳性疾病的病因。慕尼黑的一個研究小組開發了一種算法,可以預測基因突變對RNA形成的影響,比以前的模型精確6倍。因此,可以更準確地確定罕見遺傳疾病和癌癥的遺傳原因。
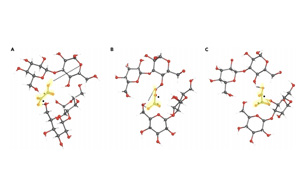
iScience首次揭開了微生物黏液的秘密
根據馬薩諸塞大學阿姆赫斯特分校與伍斯特理工學院合作的一項最新研究,一些微生物的ECM只有在草酸或其他單酸存在時才會形成凝膠。由于ECM在從抗生素耐藥性到管道堵塞和醫療器械污染的各種問題上都發揮著重要作
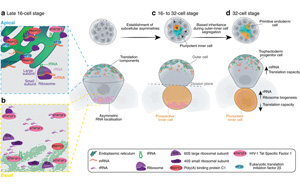
Nature子刊:RNA引導機制驅動細胞命運
胚胎發育的早期階段包含了許多生命的奧秘。解開這些謎團可以幫助我們更好地理解早期發育和出生缺陷,并幫助開發新的再生醫學治療方法。莫納什大學澳大利亞再生醫學研究所(ARMI)的研究人員利用強大而創新的成像技術描述了哺乳動物胚胎發育的關鍵時刻,他們的研究成果發表在《自然通訊》上。
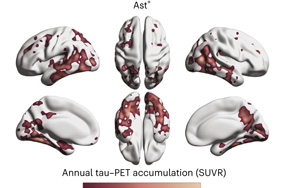
《Nature Medicine》阿爾茲海默癥新的血液生物標志物
發表在《Nature Medicine》上的一項改變游戲規則的新研究表明,被稱為星形膠質細胞的星形腦細胞是影響阿爾茨海默病進展的關鍵。
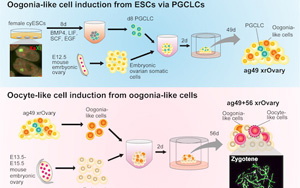
研究人員在實驗室成功地誘導了靈長類動物的卵母細胞
由Mitinori saiitou博士領導的日本研究小組的一項新研究成功地從食蟹猴的胚胎干細胞中誘導了減數分裂(分裂)卵母細胞,食蟹猴與人類有許多共同的生理特征。通過建立一種誘導減數分裂卵母細胞分化的培養方法,研究人員旨在揭示人類和其他靈長類動物生殖細胞的發育。這項研究的結果發表在2023年3月的《The EMBO Journal》上。