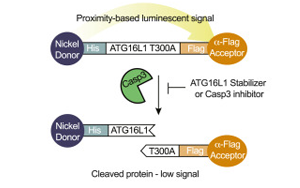
麻省理工學(xué)院博德研究所、哈佛大學(xué)、麻省總醫(yī)院和哈佛大學(xué)的研究人員采用了一種新的方法,建立了一個(gè)非常多樣化的分子化合物集合,可以以新的方式挖掘那些針對疾病相關(guān)基因變異的分子化合物。由于創(chuàng)新的化學(xué)方法,該文庫包含了超過300萬種化合物,這些化合物被設(shè)計(jì)成將兩種蛋白質(zhì)結(jié)合在一起,并使用一種作為屏障來穩(wěn)定另一種并逆轉(zhuǎn)其與疾病相關(guān)的影響。
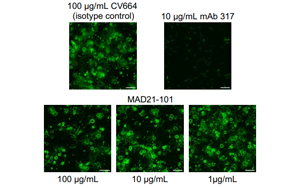
Science:一類全新的抗瘧疾抗體
根據(jù)美國國立衛(wèi)生研究院(NIH)的研究人員今天發(fā)表在《科學(xué)》雜志上的一項(xiàng)研究,一種新型抗體可以與瘧疾寄生蟲以前未靶向的部分結(jié)合,可能會(huì)導(dǎo)致新的預(yù)防方法。在美國國立衛(wèi)生研究院國家過敏和傳染病研究所(NIAID)的科學(xué)家們的帶領(lǐng)下,研究小組使用了一種新的方法來尋找抗體結(jié)合的孢子體表面的新部分或表位。他們分離出針對整個(gè)孢子蟲而不是瘧原蟲特定部分產(chǎn)生的人類單克隆抗體,然后在瘧疾小鼠模型中測試這些單克隆抗體,看它們是否能中和孢子蟲。一種名為MAD21-101的單抗被發(fā)現(xiàn)是最有效的,可以保護(hù)小鼠免受惡性瘧原蟲感染。
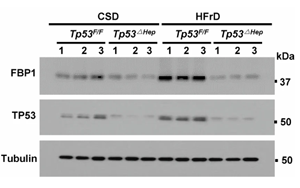
《Nature》脂肪肝為什么會(huì)導(dǎo)致肝癌?
加州大學(xué)圣地亞哥分校醫(yī)學(xué)院的科學(xué)家們對肝癌的發(fā)展有了新的了解。這項(xiàng)發(fā)表在《Nature》雜志上的研究揭示了細(xì)胞代謝和DNA損傷之間復(fù)雜的相互作用,這種相互作用推動(dòng)了脂肪肝疾病向癌癥的發(fā)展。這些發(fā)現(xiàn)為預(yù)防和治療肝癌提供了新的途徑,并對我們了解癌癥的起源和飲食對我們DNA的影響具有重要意義。
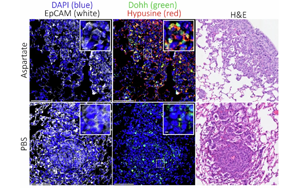
Nature:癌癥轉(zhuǎn)移時(shí)為何青睞肺部?
一項(xiàng)統(tǒng)計(jì)數(shù)據(jù)顯示,當(dāng)癌癥擴(kuò)散到原發(fā)部位以外時(shí),54%的癌癥患者會(huì)發(fā)生肺轉(zhuǎn)移。是什么讓肺部成為癌細(xì)胞如此青睞的地方?為了找出答案,比利時(shí)魯汶大學(xué)-VIB癌癥生物學(xué)中心Sarah-Maria Fendt教授領(lǐng)導(dǎo)的研究團(tuán)隊(duì)對侵襲性肺轉(zhuǎn)移瘤中細(xì)胞的基因表達(dá)進(jìn)行了深入分析。他們發(fā)現(xiàn),肺轉(zhuǎn)移與天冬氨酸有關(guān)。
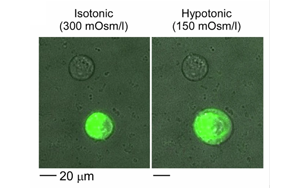
《Nature Biomedical Engineering》疼痛研究新突破:一種更安全、不會(huì)上癮的方法
新加坡國立大學(xué)(NUS)的研究人員與中國北京大學(xué)合作,發(fā)現(xiàn)了TRPV1(瞬時(shí)受體電位香草素1)離子通道及其在疼痛感知中的作用的新見解。他們的發(fā)現(xiàn)證明了溶劑分子如何影響疼痛信號,為潛在的更安全、非成癮性疼痛管理策略的發(fā)展鋪平了道路。
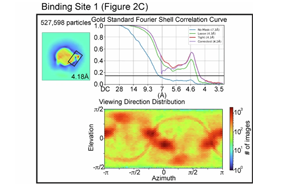
Nature里程碑成果:首次證明了“壞”膽固醇如何從血液中被清除的機(jī)制
發(fā)表在《自然》雜志上的這一研究發(fā)現(xiàn),增強(qiáng)了我們對低密度脂蛋白如何導(dǎo)致心臟病的認(rèn)識(shí)。心臟病是世界范圍內(nèi)死亡的主要原因,并可能為更有針對性的低密度脂蛋白降低療法鋪平道路,比如個(gè)性化的他汀類藥物治療,以提高其有效性。
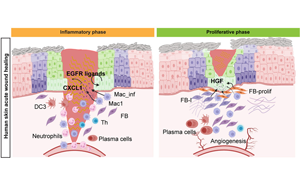
《Cell Stem Cell》單細(xì)胞解析傷口愈合的分子動(dòng)力學(xué)
卡羅林斯卡學(xué)院的一項(xiàng)新研究以非常詳細(xì)的方式描繪了人類傷口愈合的細(xì)胞和分子動(dòng)力學(xué)。這項(xiàng)研究發(fā)表在《Cell Stem Cell》雜志上。研究人員研究了同一個(gè)體在不同愈合階段的皮膚和傷口:炎癥、增殖和重塑。
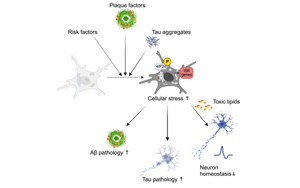
《Neuron》阿爾茨海默氏癥背后隱藏的罪魁禍?zhǔn)祝猴@微鏡下看小膠質(zhì)細(xì)胞
紐約市立大學(xué)研究生中心的研究人員在阿爾茨海默氏癥疾病研究,確定大腦細(xì)胞壓力和疾病進(jìn)展之間的關(guān)鍵聯(lián)系。他們的研究重點(diǎn)是小膠質(zhì)細(xì)胞,即大腦的免疫細(xì)胞,它在保護(hù)或損害大腦健康方面起著雙重作用。
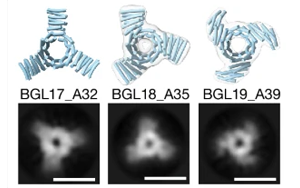
Nature:威脅人類的病毒開啟了未來
美國華盛頓大學(xué)的2024年諾貝爾化學(xué)獎(jiǎng)得主David Baker教授,與浦項(xiàng)工科大學(xué)化學(xué)工程系的Sangmin Lee教授合作,利用人工智能(AI)模擬病毒的復(fù)雜結(jié)構(gòu),開發(fā)出了一種創(chuàng)新的治療平臺(tái)。他們的開創(chuàng)性研究成果發(fā)表在了當(dāng)?shù)貢r(shí)間18日出版的《自然》雜志上。