摘要:一項(xiàng)研究報(bào)告稱(chēng),切斷癌細(xì)胞接近脂肪的途徑可能有助于一種特定類(lèi)型的癌癥治療更有效。
鐵死亡是一種由細(xì)胞磷脂氧化損傷引起的非凋亡形式的細(xì)胞死亡。為了修復(fù)這種損傷,細(xì)胞通過(guò)谷胱甘肽過(guò)氧化物酶4 (GPX4)將有毒的脂質(zhì)過(guò)氧化物還原為無(wú)毒的脂質(zhì)醇。通過(guò)抑制GPX4或阻斷抗氧化劑如谷胱甘肽和輔酶Q10的產(chǎn)生,損害脂質(zhì)過(guò)氧化物的修復(fù),導(dǎo)致細(xì)胞內(nèi)脂質(zhì)過(guò)氧化物的積累,從而誘導(dǎo)鐵死亡。由于鐵死亡與多種病理狀況有關(guān),包括癌癥、缺血-再灌注損傷和神經(jīng)退行性疾病,因此操縱鐵死亡誘導(dǎo)正在被探索作為一種新的治療策略。
含有多不飽和脂肪酸(PUFAs)的磷脂特別容易被氧化,因?yàn)樗鼈冇卸鄠€(gè)雙鍵。特別是花生四烯酸(20:4(n-6))和腎上腺酸(22:4(n-6))與某些細(xì)胞類(lèi)型的鐵死亡誘導(dǎo)有關(guān),補(bǔ)充外源性多不飽和脂肪酸可以通過(guò)將其摻入磷脂使細(xì)胞對(duì)鐵死亡敏感。飽和脂肪酸(SFA)和單不飽和脂肪酸(MUFAs)不易被氧化,向細(xì)胞提供單不飽和脂肪酸可通過(guò)從質(zhì)膜中置換含多不飽和脂肪酸的磷脂來(lái)抑制鐵死亡。基于這些結(jié)果,增加的細(xì)胞PUFA水平促進(jìn)鐵死亡敏感性,而更高的MUFA水平賦予鐵死亡抗性。癌細(xì)胞對(duì)鐵死亡誘導(dǎo)的敏感性依賴于環(huán)境,確定控制鐵死亡易感性的因素將使這一過(guò)程更好地靶向癌癥治療。
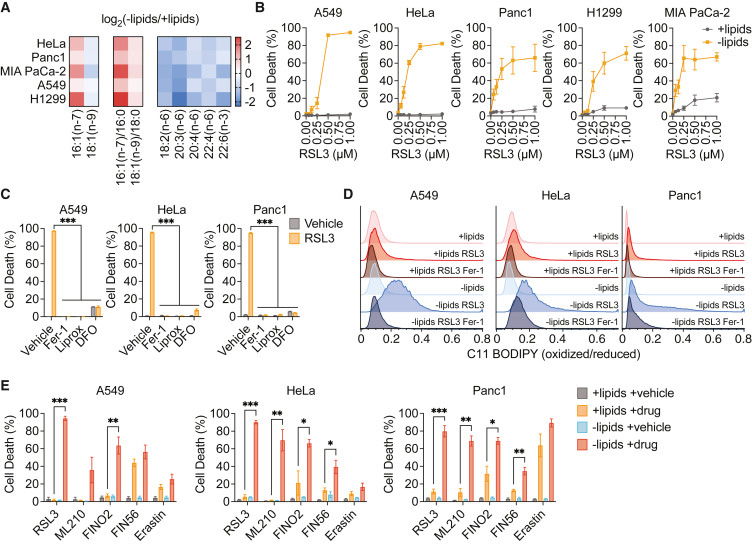
圖1 脂質(zhì)限制使癌癥細(xì)胞對(duì)脫鐵敏感
范安德?tīng)栄芯克茖W(xué)家研究發(fā)現(xiàn),切斷癌細(xì)胞獲得脂肪的途徑、限制癌細(xì)胞外脂質(zhì),可增加癌細(xì)胞對(duì)鐵死亡的敏感性,盡管可以氧化的細(xì)胞PUFAs水平降低。利用基于質(zhì)譜的脂質(zhì)組學(xué)和穩(wěn)定同位素脂肪酸標(biāo)記,作者對(duì)脂質(zhì)限制如何改變細(xì)胞脂質(zhì)代謝途徑活性進(jìn)行詳細(xì)研究,發(fā)現(xiàn)脂質(zhì)匱乏的細(xì)胞激活了PUFA運(yùn)輸途徑,在該途徑中,PUFA從TG中釋放出來(lái),轉(zhuǎn)化為高度不飽和的PUFA,并用于合成二酰基和醚類(lèi)磷脂。磷脂池中PUFAs的積累促進(jìn)了脂質(zhì)匱乏的癌細(xì)胞對(duì)鐵死亡誘導(dǎo)的敏感性。這些發(fā)現(xiàn)的一個(gè)含義是,總細(xì)胞水平的PUFAs單獨(dú)不一定預(yù)測(cè)鐵死亡的易感性。相反,脂質(zhì)重塑持續(xù)發(fā)生,部分受環(huán)境變化調(diào)節(jié),高度不飽和PUFA轉(zhuǎn)運(yùn)到適當(dāng)?shù)牧字赜兄诎┘?xì)胞對(duì)鐵死亡的敏感性。研究結(jié)果表明,降低腫瘤微環(huán)境中脂質(zhì)可用性的策略可能會(huì)提高鐵死亡誘導(dǎo)劑治療癌癥的療效。該研究結(jié)果發(fā)表在《Cell Chemical Biology》雜志上,為開(kāi)發(fā)量身定制的飲食策略奠定了基礎(chǔ),以幫助抗癌藥物更好地殺死惡性細(xì)胞。
VAI助理教授,該研究的通訊作者Evan Lien博士說(shuō):“我們想讓癌癥治療更有效。要做到這一點(diǎn),最好的方法是了解癌細(xì)胞的行為方式,并找出突破它們防御的方法。我們的發(fā)現(xiàn)是朝著循證飲食邁出的重要一步,有朝一日,這種飲食可能會(huì)增強(qiáng)現(xiàn)有的治療方法。”
脂肪是維持健康機(jī)能所必需的關(guān)鍵營(yíng)養(yǎng)素。癌細(xì)胞劫持正常的細(xì)胞過(guò)程,竊取脂肪等資源,然后作為病態(tài)細(xì)胞生長(zhǎng)和擴(kuò)散的燃料。許多使癌細(xì)胞不受控制地生長(zhǎng)的機(jī)制也使它們能夠避免通常殺死和清除病態(tài)細(xì)胞的細(xì)胞質(zhì)量控制過(guò)程。鐵死亡可能是一個(gè)例外,這使得它成為癌癥治療中潛在的強(qiáng)大工具。利用細(xì)胞模型,Lien和他的團(tuán)隊(duì)表明,去除癌細(xì)胞獲取脂肪的途徑,使它們對(duì)鐵死亡高度敏感,可進(jìn)而對(duì)誘導(dǎo)鐵死亡的藥物高度敏感。

圖2 脂質(zhì)可利用性通過(guò)調(diào)節(jié)多不飽和脂肪酸轉(zhuǎn)運(yùn)影響癌癥細(xì)胞的脫鐵敏感性
Lien說(shuō),這些發(fā)現(xiàn)很有希望,但要在其他癌癥模型中復(fù)制這一發(fā)現(xiàn),還需要做更多的工作。他和他的團(tuán)隊(duì)還在研究是否可以通過(guò)飲食來(lái)控制脂肪的類(lèi)型和數(shù)量,從而使鐵死亡誘導(dǎo)劑更有效地發(fā)揮作用。
“飲食是相對(duì)容易改變的東西,”Lien說(shuō)。“我們還沒(méi)有做到這一點(diǎn),但我們最興奮的是,我們?nèi)绾文軌蚶梦覀兯鶎W(xué)到的東西,有一天設(shè)計(jì)出適合不同類(lèi)型治療的飲食。這可能會(huì)帶來(lái)變革。”
參考資料
[1] Lipid availability influences ferroptosis sensitivity in cancer cells by regulating polyunsaturated fatty acid trafficking
摘要:一項(xiàng)研究報(bào)告稱(chēng),切斷癌細(xì)胞接近脂肪的途徑可能有助于一種特定類(lèi)型的癌癥治療更有效。
鐵死亡是一種由細(xì)胞磷脂氧化損傷引起的非凋亡形式的細(xì)胞死亡。為了修復(fù)這種損傷,細(xì)胞通過(guò)谷胱甘肽過(guò)氧化物酶4 (GPX4)將有毒的脂質(zhì)過(guò)氧化物還原為無(wú)毒的脂質(zhì)醇。通過(guò)抑制GPX4或阻斷抗氧化劑如谷胱甘肽和輔酶Q10的產(chǎn)生,損害脂質(zhì)過(guò)氧化物的修復(fù),導(dǎo)致細(xì)胞內(nèi)脂質(zhì)過(guò)氧化物的積累,從而誘導(dǎo)鐵死亡。由于鐵死亡與多種病理狀況有關(guān),包括癌癥、缺血-再灌注損傷和神經(jīng)退行性疾病,因此操縱鐵死亡誘導(dǎo)正在被探索作為一種新的治療策略。
含有多不飽和脂肪酸(PUFAs)的磷脂特別容易被氧化,因?yàn)樗鼈冇卸鄠€(gè)雙鍵。特別是花生四烯酸(20:4(n-6))和腎上腺酸(22:4(n-6))與某些細(xì)胞類(lèi)型的鐵死亡誘導(dǎo)有關(guān),補(bǔ)充外源性多不飽和脂肪酸可以通過(guò)將其摻入磷脂使細(xì)胞對(duì)鐵死亡敏感。飽和脂肪酸(SFA)和單不飽和脂肪酸(MUFAs)不易被氧化,向細(xì)胞提供單不飽和脂肪酸可通過(guò)從質(zhì)膜中置換含多不飽和脂肪酸的磷脂來(lái)抑制鐵死亡。基于這些結(jié)果,增加的細(xì)胞PUFA水平促進(jìn)鐵死亡敏感性,而更高的MUFA水平賦予鐵死亡抗性。癌細(xì)胞對(duì)鐵死亡誘導(dǎo)的敏感性依賴于環(huán)境,確定控制鐵死亡易感性的因素將使這一過(guò)程更好地靶向癌癥治療。

圖1 脂質(zhì)限制使癌癥細(xì)胞對(duì)脫鐵敏感
范安德?tīng)栄芯克茖W(xué)家研究發(fā)現(xiàn),切斷癌細(xì)胞獲得脂肪的途徑、限制癌細(xì)胞外脂質(zhì),可增加癌細(xì)胞對(duì)鐵死亡的敏感性,盡管可以氧化的細(xì)胞PUFAs水平降低。利用基于質(zhì)譜的脂質(zhì)組學(xué)和穩(wěn)定同位素脂肪酸標(biāo)記,作者對(duì)脂質(zhì)限制如何改變細(xì)胞脂質(zhì)代謝途徑活性進(jìn)行詳細(xì)研究,發(fā)現(xiàn)脂質(zhì)匱乏的細(xì)胞激活了PUFA運(yùn)輸途徑,在該途徑中,PUFA從TG中釋放出來(lái),轉(zhuǎn)化為高度不飽和的PUFA,并用于合成二酰基和醚類(lèi)磷脂。磷脂池中PUFAs的積累促進(jìn)了脂質(zhì)匱乏的癌細(xì)胞對(duì)鐵死亡誘導(dǎo)的敏感性。這些發(fā)現(xiàn)的一個(gè)含義是,總細(xì)胞水平的PUFAs單獨(dú)不一定預(yù)測(cè)鐵死亡的易感性。相反,脂質(zhì)重塑持續(xù)發(fā)生,部分受環(huán)境變化調(diào)節(jié),高度不飽和PUFA轉(zhuǎn)運(yùn)到適當(dāng)?shù)牧字赜兄诎┘?xì)胞對(duì)鐵死亡的敏感性。研究結(jié)果表明,降低腫瘤微環(huán)境中脂質(zhì)可用性的策略可能會(huì)提高鐵死亡誘導(dǎo)劑治療癌癥的療效。該研究結(jié)果發(fā)表在《Cell Chemical Biology》雜志上,為開(kāi)發(fā)量身定制的飲食策略奠定了基礎(chǔ),以幫助抗癌藥物更好地殺死惡性細(xì)胞。
VAI助理教授,該研究的通訊作者Evan Lien博士說(shuō):“我們想讓癌癥治療更有效。要做到這一點(diǎn),最好的方法是了解癌細(xì)胞的行為方式,并找出突破它們防御的方法。我們的發(fā)現(xiàn)是朝著循證飲食邁出的重要一步,有朝一日,這種飲食可能會(huì)增強(qiáng)現(xiàn)有的治療方法。”
脂肪是維持健康機(jī)能所必需的關(guān)鍵營(yíng)養(yǎng)素。癌細(xì)胞劫持正常的細(xì)胞過(guò)程,竊取脂肪等資源,然后作為病態(tài)細(xì)胞生長(zhǎng)和擴(kuò)散的燃料。許多使癌細(xì)胞不受控制地生長(zhǎng)的機(jī)制也使它們能夠避免通常殺死和清除病態(tài)細(xì)胞的細(xì)胞質(zhì)量控制過(guò)程。鐵死亡可能是一個(gè)例外,這使得它成為癌癥治療中潛在的強(qiáng)大工具。利用細(xì)胞模型,Lien和他的團(tuán)隊(duì)表明,去除癌細(xì)胞獲取脂肪的途徑,使它們對(duì)鐵死亡高度敏感,可進(jìn)而對(duì)誘導(dǎo)鐵死亡的藥物高度敏感。

圖2 脂質(zhì)可利用性通過(guò)調(diào)節(jié)多不飽和脂肪酸轉(zhuǎn)運(yùn)影響癌癥細(xì)胞的脫鐵敏感性
Lien說(shuō),這些發(fā)現(xiàn)很有希望,但要在其他癌癥模型中復(fù)制這一發(fā)現(xiàn),還需要做更多的工作。他和他的團(tuán)隊(duì)還在研究是否可以通過(guò)飲食來(lái)控制脂肪的類(lèi)型和數(shù)量,從而使鐵死亡誘導(dǎo)劑更有效地發(fā)揮作用。
“飲食是相對(duì)容易改變的東西,”Lien說(shuō)。“我們還沒(méi)有做到這一點(diǎn),但我們最興奮的是,我們?nèi)绾文軌蚶梦覀兯鶎W(xué)到的東西,有一天設(shè)計(jì)出適合不同類(lèi)型治療的飲食。這可能會(huì)帶來(lái)變革。”
參考資料
[1] Lipid availability influences ferroptosis sensitivity in cancer cells by regulating polyunsaturated fatty acid trafficking



